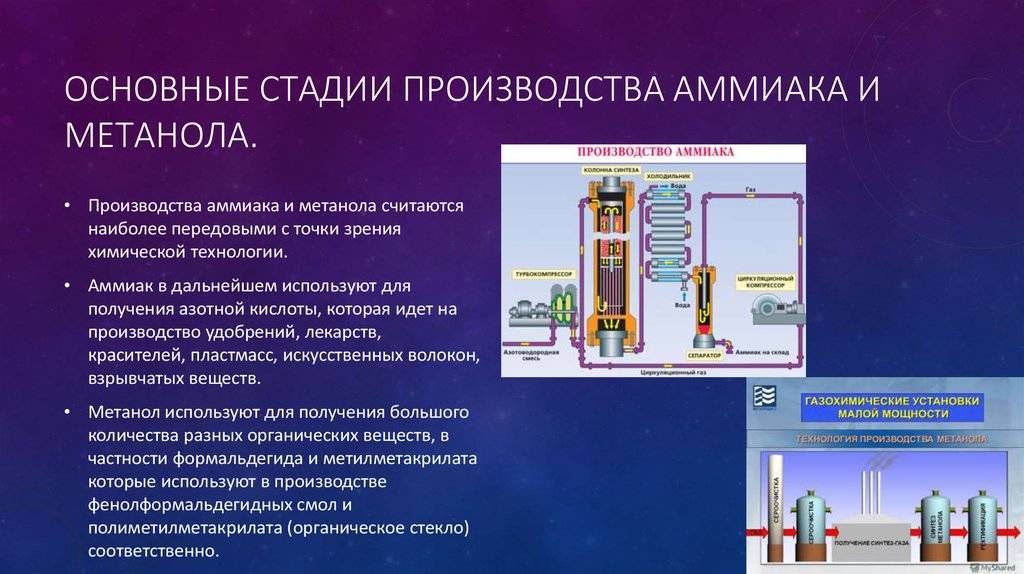
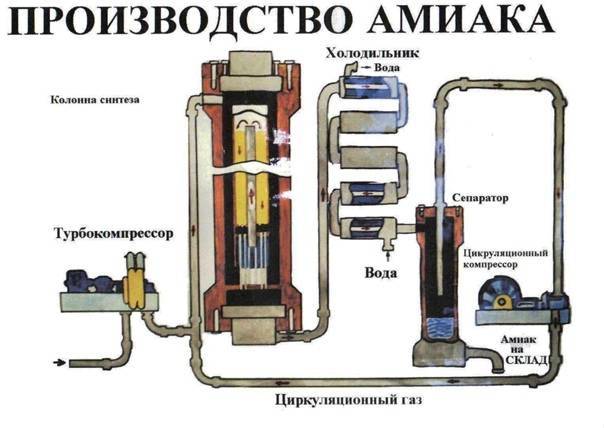
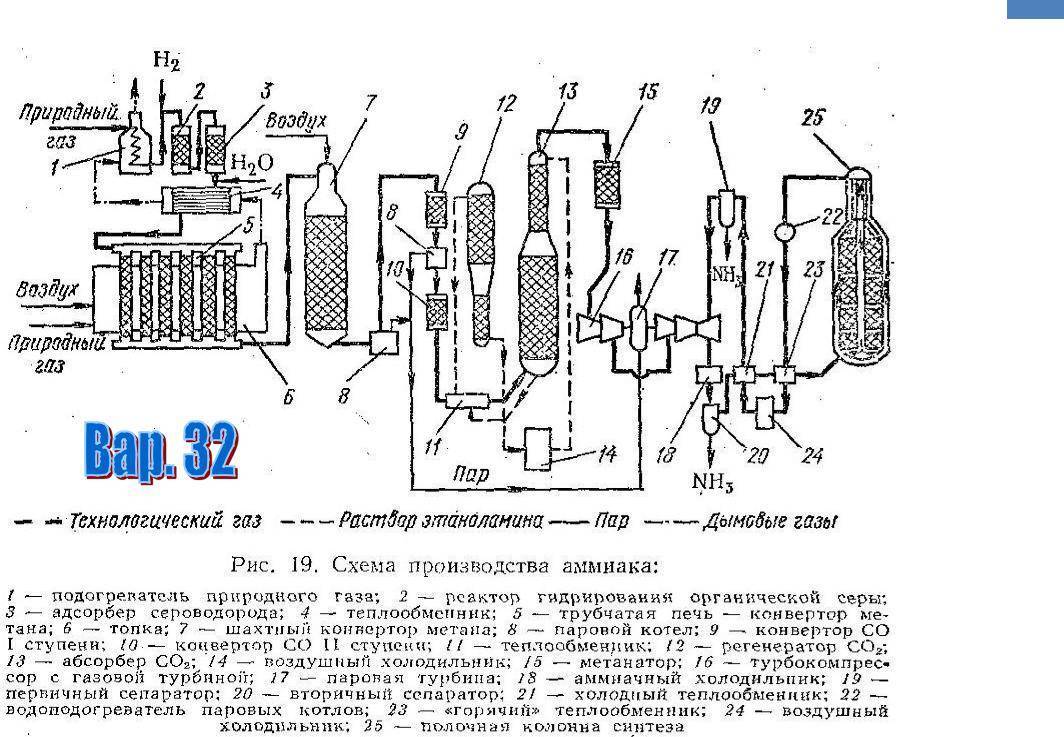
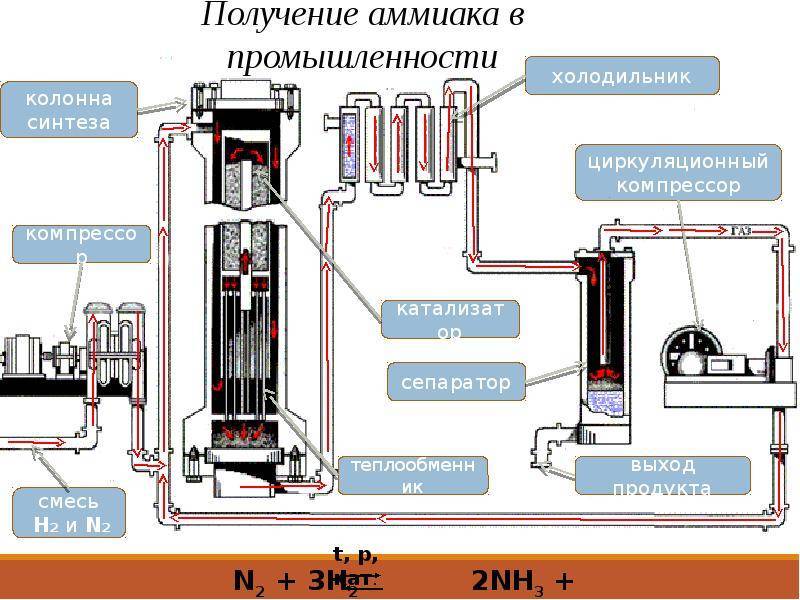
Получение вещества в лаборатории
Первый метод получения аммиака заключается в доведении нашатырного спирта до кипения, после чего полученный пар осушают и собирают требуемое химическое соединение. Получение аммиака в лаборатории возможно также путем нагревания гашеной извести и твердого хлорида аммония.
Реакция получения аммиака имеет такой вид:
2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3 + 2H2O
В ходе этой реакции выпадает осадок белого цвета. Это соль CaCl2, а еще образовывается вода и искомый аммиак. Для проведения осушения требуемого вещества его пропускают по смеси извести в сочетании с натром.
Получение аммиака в лаборатории не обеспечивает самую оптимальную технологию его производства в необходимых количествах. Люди много лет искали способы добычи вещества в промышленных масштабах.
Производство серной кислоты
В качестве серосодержащего сырья для производства серной кислоты могут быть использованы сера или сероводород (побочные продукты нефтепереработки), минерал пирит FeS2, а также сульфиды некоторых других d-элементов. Никакие другие виды сырья не используются.
В настоящий момент основным сырьем для производства серной кислоты являются сероводород и сера, поскольку они в огромных количествах образуются в качестве побочных продуктов нефтепереработки.
Однако же в школьной программе пока еще по-прежнему считается, что серная кислота производится преимущественно из пирита, в связи с чем и мы будем рассматривать основные стадии производства серной кислоты именно этого же сырья.
Первая стадия
Заключается в сжигании предварительно измельченного пирита в токе обогащенного кислородом воздуха. Процесс протекает в соответствии с уравнением:
Обжиг осуществляют при температуре около 800 оС в печи для обжига. В процессе обжига используют так называемый метод кипящего слоя – частицы измельченного пирита подаются в печь сверху, а воздух — снизу. В результате этого раскаленные частицы пирита оказываются подвешенными в токе воздуха, внешне напоминая кипящую жидкость.
После обжига пирита полученный печной газ, содержащий диоксид серы, отделяется от твердых примесей огарка (Fe2O3) с помощью циклона. Циклоном называют аппарат, в котором происходит грубая очистка печных газов за счет центробежной силы от наиболее крупных твердых частиц. Далее после грубой очистки смесь газов проходит более глубокую очистку уже от оставшихся мелких твердых частиц с помощью электрофильтра. Принцип действия электрофильтра основан на том, что к наэлектризованным металлическим пластинам прилипает пыль, которая после скопления ссыпается с них под собственным весом в приемник.
После очистки от твердых примесей печной газ направляется в нижнюю часть так называемой сушильной башни, в верхнюю часть которой впрыскивается концентрированная серная кислота на встречу газу. При таком варианте осуществления фактически сталкиваются два потока — смеси газов, идущей снизу, и струи жидкой концентрированной серной кислоты, текущей сверху. Очевидно, что в результате этого достигается максимальная степень «смешения» газа с осушающей жидкостью. Данный прием носит название принципа противотока.
Вторая стадия
После очистки от твердых примесей и осушки концентрированной серной кислотой газы поступают в контактный аппарат. В контактном аппарате расположены полки с катализатором V2O5, который катализирует взаимодействие диоксида серы с кислородом в соответствии с уравнением:
Аналогично реакции взаимодействия азота с водородом, рассмотренной выше, данная реакция также является каталитической, экзотермической и протекает с уменьшением количества газообразных веществ. Поэтому с точки зрения принципа Ле Шателье ее следовало бы проводить при низких температурах. Однако при низких температурах скорость реакции крайне низка, и ее осуществляют при оптимальной температуре около 400-500 оС. Смещения равновесия реакции в сторону разложения SO3 при повышении температуры удается практически полностью избежать, проводя реакцию при повышенном давлении.
Третья стадия (заключительная)
После второй стадии образовавшийся триоксид серы поступает в часть установки, называемую поглотительной башней.
Из названия данного аппарата логичным было бы предположить, что триоксид серы в нем поглощается в этой части установки водой, ведь триоксид серы, взаимодействуя с водой, образует серную кислоту. Однако в реальности серный ангидрид SO3поглощают не водой (!!!), а концентрированной серной кислотой. Связано это с тем, что при смешении серного ангидрида с водой выделяется колоссальное количество теплоты, в результате чего сильно возрастают температура, давление и образуются мельчайшие капли трудноуловимого сернокислотного тумана.
В результате поглощения SO3 концентрированной серной кислотой фактически образуется раствор SO3 в безводной серной кислоте, который называют олеумом. Далее образующийся олеум собирается в металлические емкости и отправляется на склад. Серную кислоту необходимой концентрации получают, добавляя к олеуму воду в нужной пропорции. В результате добавления воды избыток SO3 превращается в серную кислоту.
Каналы сбыта выпускаемой продукции.
Для того, чтобы наладить сбыть производимых удобрений, необходимо отыскать постоянных клиентов. В этом вам не обойтись без рекламной кампании. Наиболее доступным и распространённым способом является Всемирная паутина. Разместите объявления на известных ресурсах, посвящённых строительству. Оптимальным решением для привлечения клиентов станет создание собственного сайта, на котором потребители смогут получить исчерпывающую информацию о вашей продукции. Расходы на создание и запуск собственного сайта составят около 20000 руб.
Подведем итоги и определим итоговую сумму, необходимую для первоначальных инвестиций:
- Расходы на приобретение необходимого оборудования — 13700000 руб.
- Покупка участка и помещения цеха — 3000000 руб.
- Рекламная компания —20000 руб.
- Приобретение сырья (300 тонн) — 1500000 руб.
Итоговая сумма стартового капитала — 18220000 руб. По приблизительным подсчётам себестоимость тонны произведённого удобрения составляет 7000 руб. Среднерыночная цена гранулированного карбамида составляет 15000 руб. Если реализовывать 100 тонн произведённого удобрения ежемесячно, то чистый доход будет равен 800000 руб. Исходя из этого можно сделать вывод, что окупаемость первоначальных инвестиций наступает за 1.8 года.
В промышленности
Аммиак промышленным путём получают из азота, соединяя его с водородом. Азот берут из воздуха, водород – из воды. Впервые метод разработал немецкий химик Фриц Габер. Промышленный способ получения аммиака стали называть процессом Габера.
Реакция проходит с уменьшением объёма и выделением энергии в виде тепла:
3H2 + N2 → 2NH3 + Q.
Реакция обратима, поэтому необходимо соблюсти несколько условий. При высоком давлении и низких температурах объём полученного аммиака увеличивается. Однако низкие температуры замедляют скорость реакции, а повышение температуры способствует увеличению скорости обратной реакции.
Опытным путём были найдены необходимые условия для проведения реакции:
- температура – 500°C;
- давление – 350 атм;
- катализатор – оксид железа Fe3O4 (магнетит) с примесями оксидов серебра, калия, кальция и других веществ.
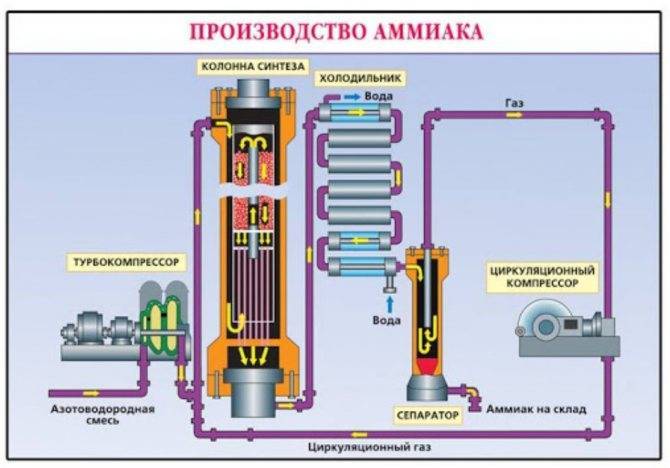
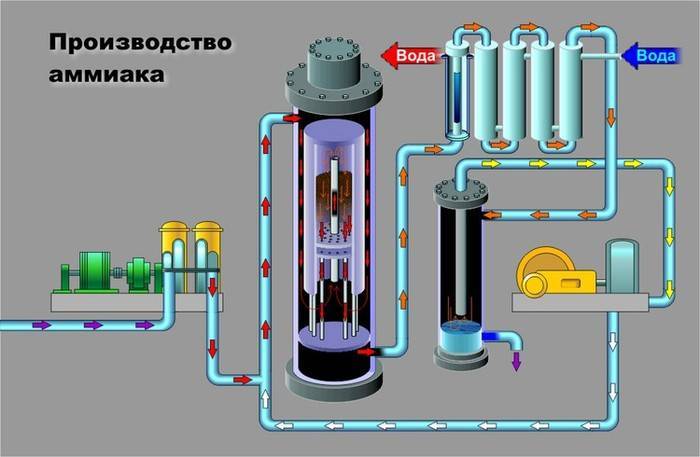
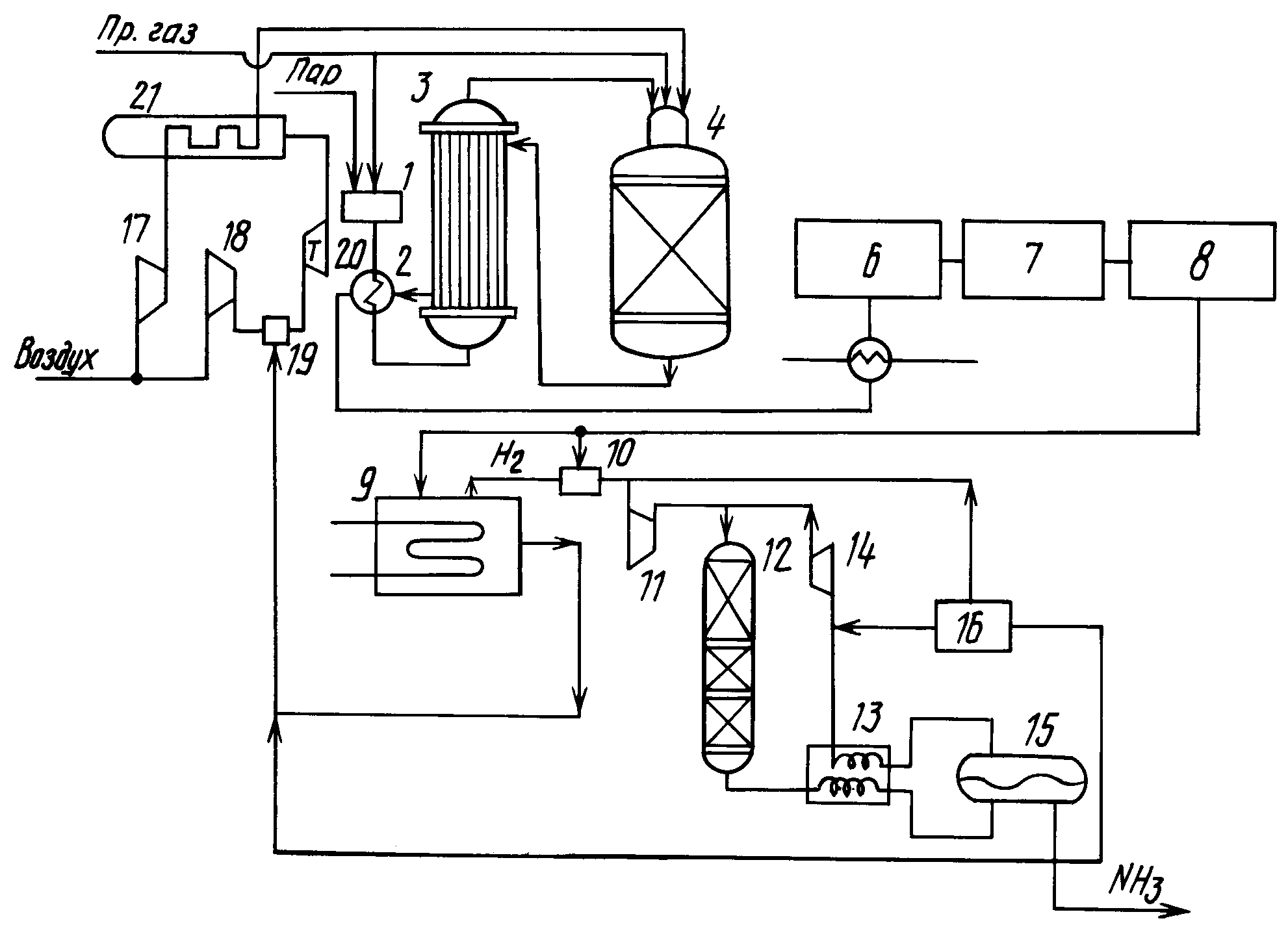
При таких условиях получившийся газ содержит 30 % аммиака. Чтобы избежать обратной реакции, вещество быстро охлаждают. При низких температурах получившийся газ превращается в жидкость. Неизрасходованные газы – азот и водород – возвращаются обратно в колонну для синтеза. Такой способ помогает быстро получить большие объёмы аммиака, максимально используя сырьё.
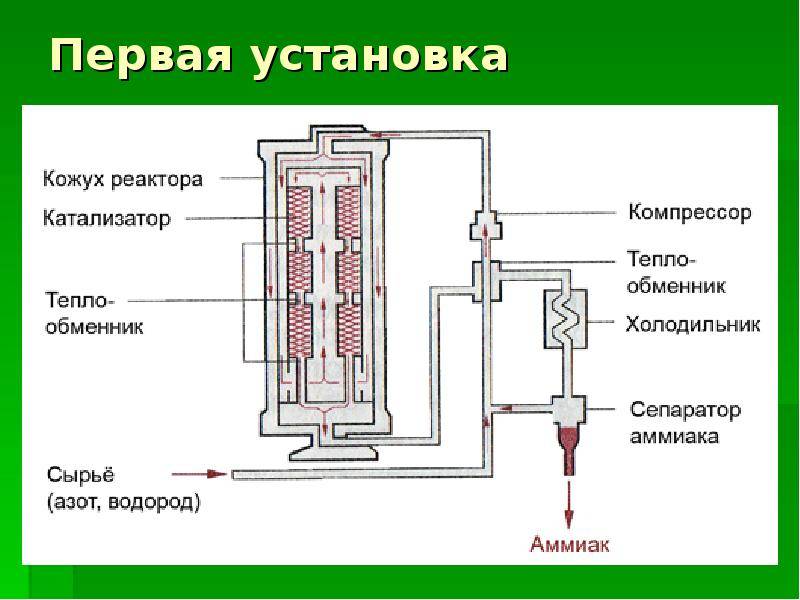
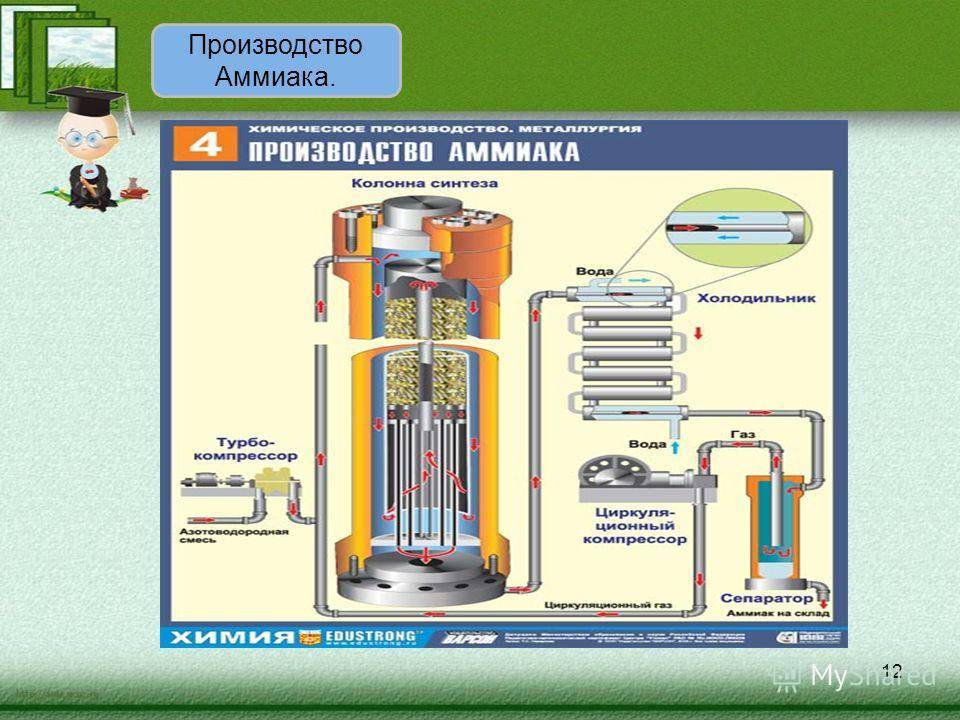
Рис. 1. Получение аммиака промышленным путём.
Чтобы найти нужный катализатор, было испробовано 20 тысяч разных веществ.
Современные заводы по производству аммиака [ править ]
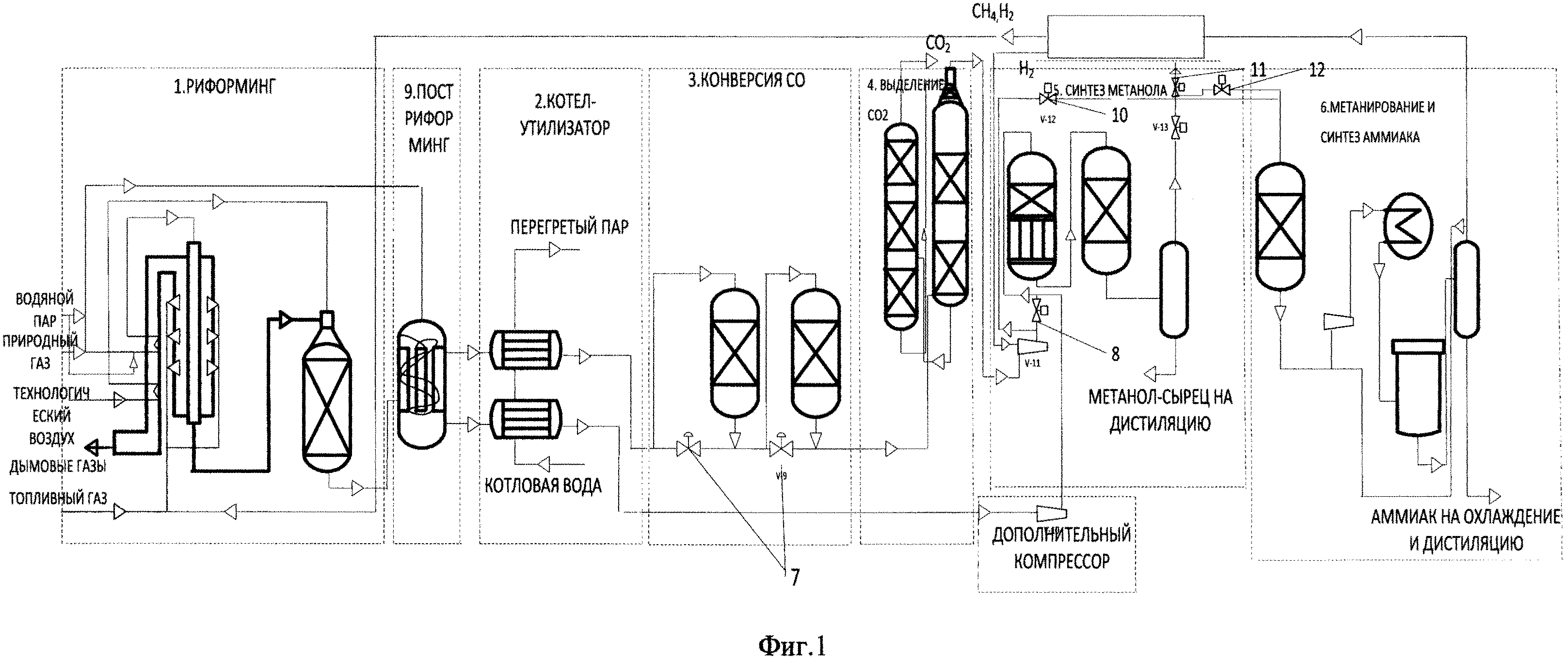
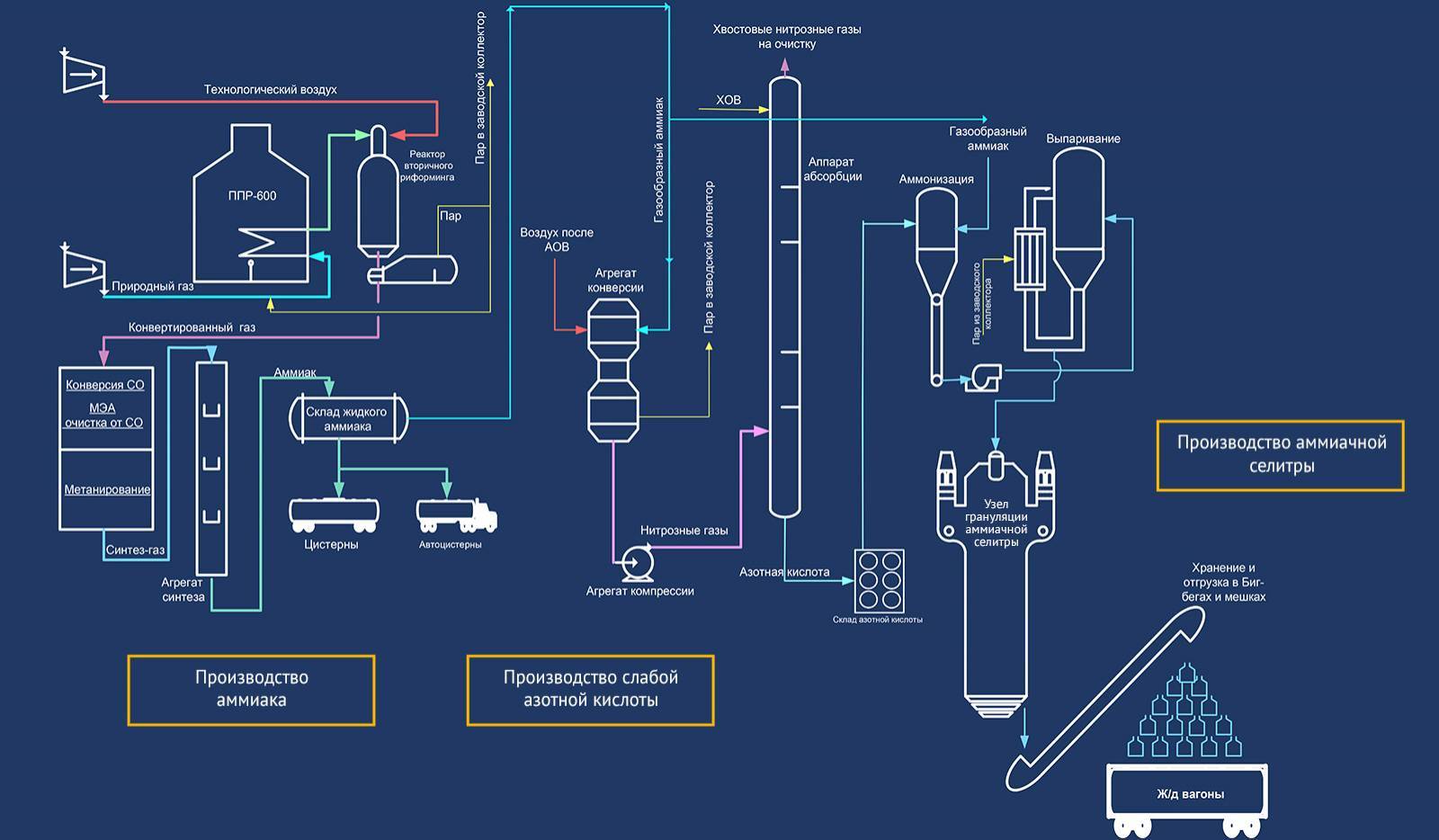
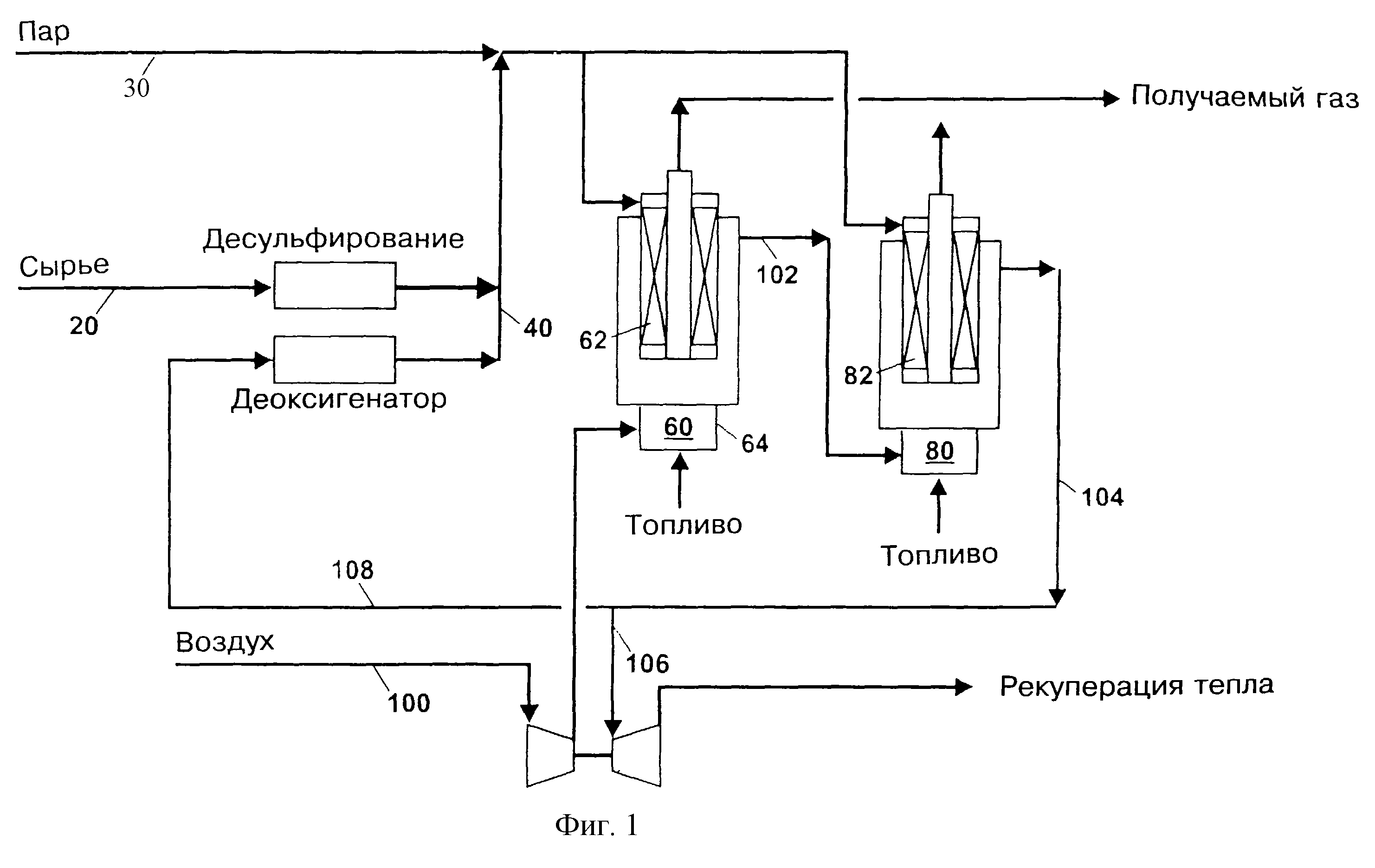
Типичная современная установка по производству аммиака сначала преобразует природный газ , сжиженный нефтяной газ или нефтяную нафту в газообразный водород . Способ получения водорода из углеводородов известен как паровой риформинг . Затем водород объединяется с азотом для получения аммиака с помощью процесса Габера-Боша .
Начиная с исходного природного газа, для производства водорода используются следующие процессы:
Первым этапом процесса является удаление соединений серы из сырья, поскольку сера дезактивирует катализаторы, используемые на последующих этапах. Удаление серы требует каталитического гидрирования для превращения соединений серы в исходном сырье в газообразный сероводород :
- H 2 + RSH → RH + H 2 S (газ)
Затем газообразный сероводород адсорбируется и удаляется, пропуская его через слои оксида цинка, где он превращается в твердый сульфид цинка :
Иллюстрируя входы и выходы парового риформинга природного газа, процесса производства водорода.
- Н 2 S + ZnO → ZnS + H 2 O
Затем используется каталитический паровой риформинг сырья, не содержащего серы, для образования водорода плюс монооксида углерода :
- СН 4 + Н 2 О → СО + 3Н 2
На следующем этапе используется преобразование каталитического сдвига для преобразования моноксида углерода в диоксид углерода и больше водорода:
- СО + Н 2 О → СО 2 + Н 2
- Затем диоксид углерода удаляют либо абсорбцией водными растворами этаноламина, либо адсорбцией в адсорберах с переменным давлением (PSA) с использованием запатентованных твердых адсорбционных сред.
- Последним шагом в производстве водорода является использование каталитического метанирования для удаления любых небольших остаточных количеств монооксида углерода или диоксида углерода из водорода:
- CO + 3H 2 → CH 4 + H 2 O
- СО 2 + 4Н 2 → СН 4 + 2Н 2 О
Для получения желаемого конечного продукта аммиака водород затем каталитически реагирует с азотом (полученным из технологического воздуха) с образованием безводного жидкого аммиака. Этот этап известен как цикл синтеза аммиака (также называемый процессом Габера-Боша ):
- 3Н 2 + N 2 → 2NH 3
Из-за природы катализатора (обычно с множественным промотированием магнетита), используемого в реакции синтеза аммиака, при синтезе могут быть допустимы только очень низкие уровни кислородсодержащих (особенно CO, CO 2 и H 2 O) соединений (водород и азотная смесь) газ. Относительно чистый азот можно получить путем разделения воздуха , но может потребоваться дополнительное удаление кислорода.
Из-за относительно низких степеней конверсии за один проход (обычно менее 20%) требуется большой поток рециркуляции. Это может привести к накоплению инертных газов в петлевом газе.
Каждая из стадий парового риформинга, сдвигового преобразования, удаления диоксида углерода и метанирования работает при абсолютном давлении примерно от 25 до 35 бар, а контур синтеза аммиака работает при абсолютном давлении в диапазоне от 60 до 180 бар в зависимости от используемой запатентованной конструкции. Есть много инженерных и строительных компаний, которые предлагают собственные разработки для установок синтеза аммиака. Хальдор Топсе из Дании, Thyssenkrupp Industrial Solutions GmbH из Германии, Ammonia Casale из Швейцарии и Kellogg Brown & Root из США являются одними из наиболее опытных компаний в этой области.
Особенности и этапы производственного процесса
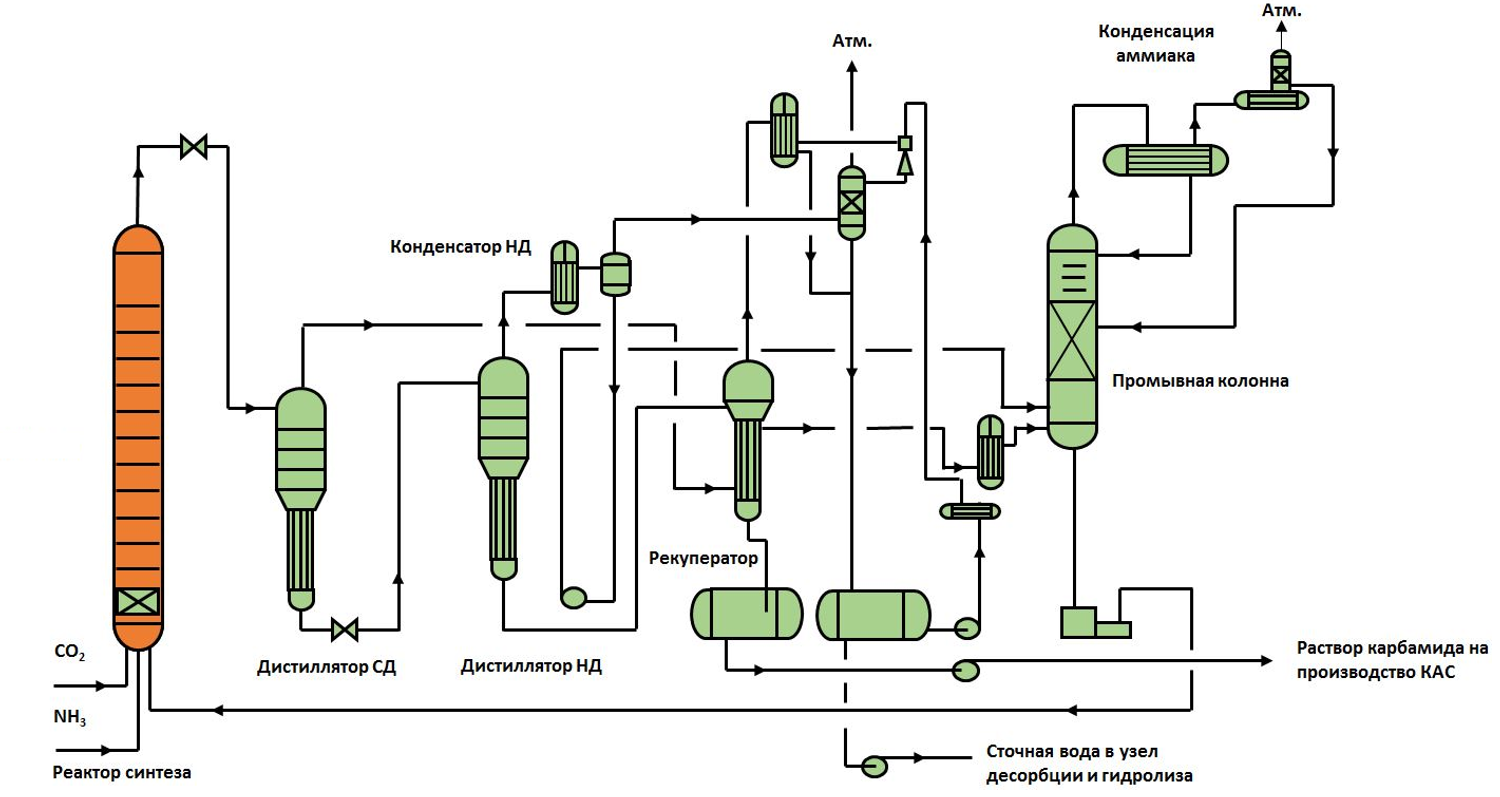
Процесс производства аммиака характеризуется большой энергоемкостью, что является главным его недостатком. Именно поэтому постоянно ведутся научные разработки, которые призваны решить проблемы экономии энергии. В частности разрабатываются способы утилизации выделенной энергии, а также совмещение, например, производства аммиака и карбамида. Все это способствует удешевлению деятельности предприятий и повышению их полезной отдачи.
В основу производства аммиака положены принцип циркуляции, согласно которому процесс идет непрерывно, причем остатки исходных компонентов отделяются от конечного продукта и используются вновь, непрерывности: процесс синтеза происходит без остановки, принцип теплообмена, а также принцип цикличности. Как видно, все эти принципы между собой тесно взаимосвязаны.

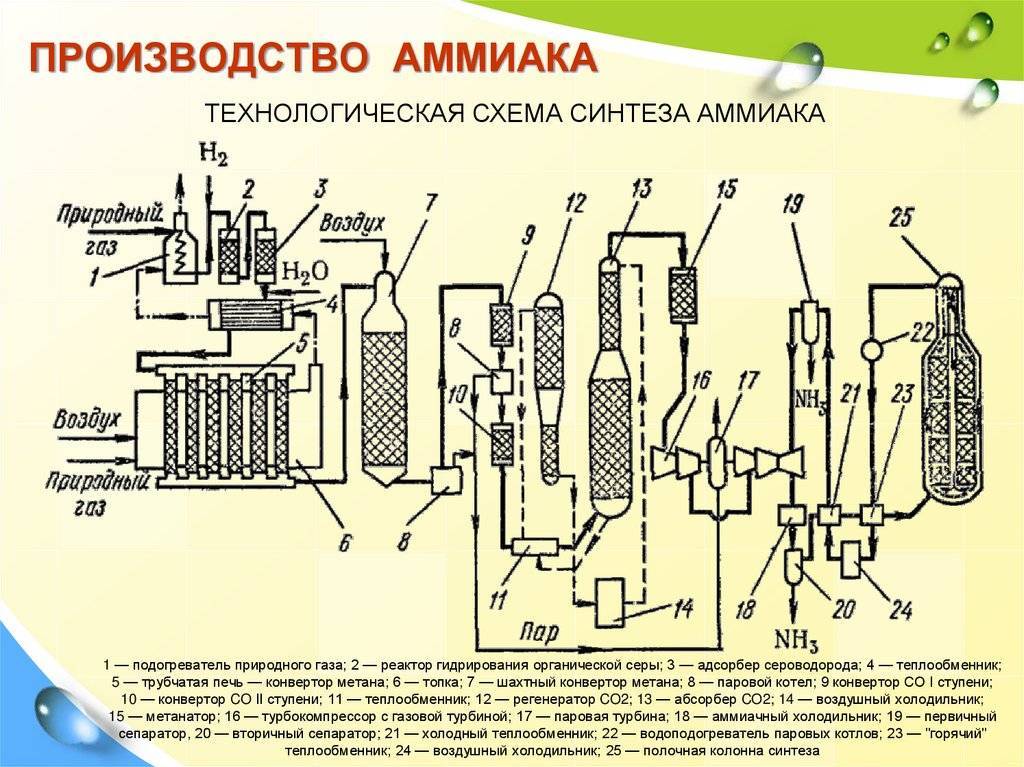
Сама технологическая схема производства аммиака зависит, прежде всего, от сырья, из которого получается конечный продукт. Дело в том, что, в отличие от азота, который содержится в воздухе в больших количествах, водород в чистом виде в природе практически не присутствует, а выделять его из воды — довольно трудоемкий и энергозатратный процесс.
Поэтому в качестве сырья для производства аммиака в основном используются углеводороды, содержащиеся в природном газе. В настоящее время именно природный газ является одной из основ аммиачной промышленности. Прежде чем попасть в колонну синтеза, газ проходит несколько стадий обработки. Начинается процесс с того что производится очистка исходного сырья от серы при помощи десульфуратора.
Далее идет так называемый процесс риформинга, который заключается в том, что в его ходе углеводороды сначала превращаются в метан, потом происходит довольно сложный процесс превращения метана в смесь водяного пара, угарного газа, углекислого газа и водорода. При этом также происходит очистка смеси от углекислого газа, после чего водород попадает в колонну синтеза под большим давлением вместе с азотом. Таким образом, прежде чем начать непосредственно производство аммиака, технология предполагает предварительную обработку сырья.

Все процессы риформинга, как и непосредственно сам синтез конечного продукта, происходят при высоком давлении и большой температуре. Именно это приводит к большой их энергозатратности. При этом указанные параметры на всех стадиях производства изменяются.
Сама колонна обычно изготавливается из стали. В ней размещен катализатор, состав которого может быть разным. После прохождения цикла синтеза смесь попадает в холодильник, где от нее оделяется аммиак в жидком виде, а оставшиеся после реакции компоненты снова идут в производство. Такая особенность технологического процесса вызвана тем, что реакция синтеза аммиака является обратимой и в ходе технологического процесса часть конечного продукта распадается на исходные компоненты.
Таким образом, производство аммиака в промышленности, несмотря на кажущуюся простоту реакции, которая лежит в основе процесса, на самом деле является довольно сложной технологической задачей.
Как организовать бизнес
Для организации работы предприятия нужно зарегистрировать свое дело, найти подходящую землю для строительства.
Перед выполнением практических действий стоит уделить внимание планированию – сформировать проект завода и бизнес-план. В последнем одним из основных разделов будет материальный – там вы укажите ожидаемые растраты на запуск и доходы
Регистрация
По сравнению с небольшим бизнесом, для которого обычно оформляется ИП, для запуска объекта среднего или большего бизнеса более подходит форма ООО.Еще необходимо получить разрешительную документацию на работу предприятия. Для этого ваша продукция должна соответствовать ГОСТу.
Потребуются и разрешительные бумаги от пожарной службы, СЭС, Росприроднадзора, налоговой службы. Договора с рабочими завода должны соответствовать ст. 56-57 и 67 ТК.
Получение всех нужных документов может затянуться на долгие годы. Лучше всего делегировать хотя бы часть этого процесса квалифицированным сотрудникам.
Выбор помещения и оборудования
При выборе земли для строительства завода нужно учесть, что это шумное и опасное производство, поэтому стоит подобрать место за чертой города. Для работы предприятия потребуется подключение к электрической сети, системе водоснабжения и водоотведения, телефонной и интернет связи.
Для удобства перевозки продукции, предприятие должно находиться рядом с удобной дорожной развязкой. Для того, чтобы запустить бизнес-проект по созданию аммиака, понадобятся следующие аппараты:
- Грануляционная башня, которая стоит примерно 10000000 рублей.
- Гранулятор, с ценников 1200000 рублей.
- Специальный насос для подачи, стоимостью 400000 рублей.
- Дутьевой вентилятор, который стоит 1600000 руб.
- Погрузчик с ценником 500000 руб.
Очевидно, бизнес требует больших вложений. В общем, исходя из отзывов опытных дельцов, производство аммиака обойдётся в сумму от 400 миллионов долларов. Окупается ли это дело? Себестоимость производства тонны аммиака в РФ оценивается в 130-160 $. А средняя стоимость продажи при этом – 250-300 долларов. На основании этой информации можно сделать вывод: бизнес этот однозначно прибыльный и выгодный.
Персонал
Грануляционного типа башню ежедневно должны обслуживать шесть специально обученных работников. Упаковывать, грузить товар и выполнять иные манипуляции будут четверо разнорабочих.
Не обойтись здесь без бухгалтера и директора.Ежемесячные расходы на выплату заработных плат составят:
- Разнорабочий — 15000 рублей.
- Мастер по ремонту агрегатов — 20000 рублей.
- Сотрудник, занимающийся бухгалтерской отчетностью — 20000 рублей.
- Руководитель — 35000 руб.
Итоговая сумма расходов на зарплату всего 365000 рублей.
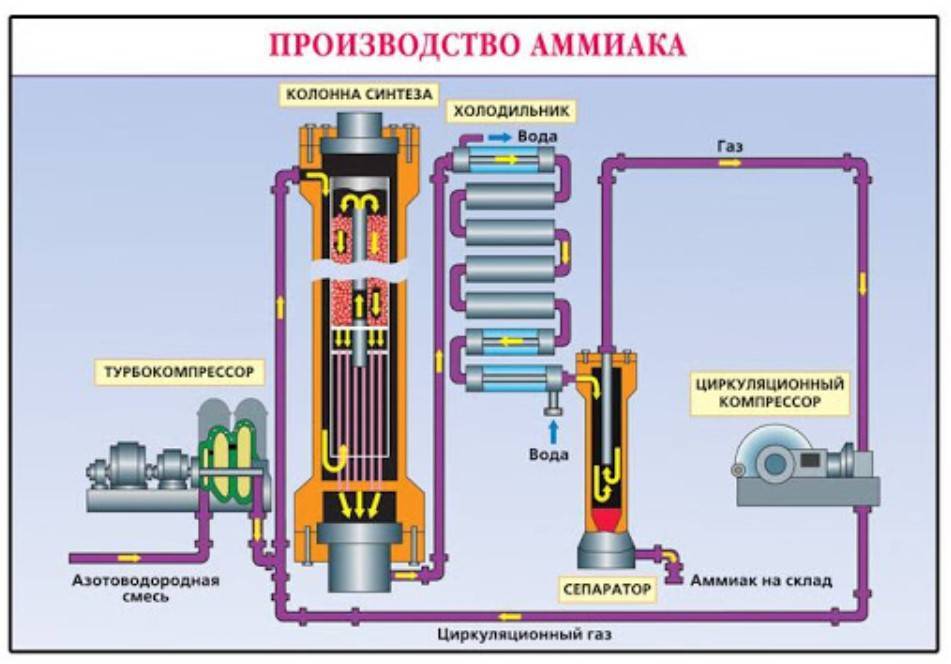
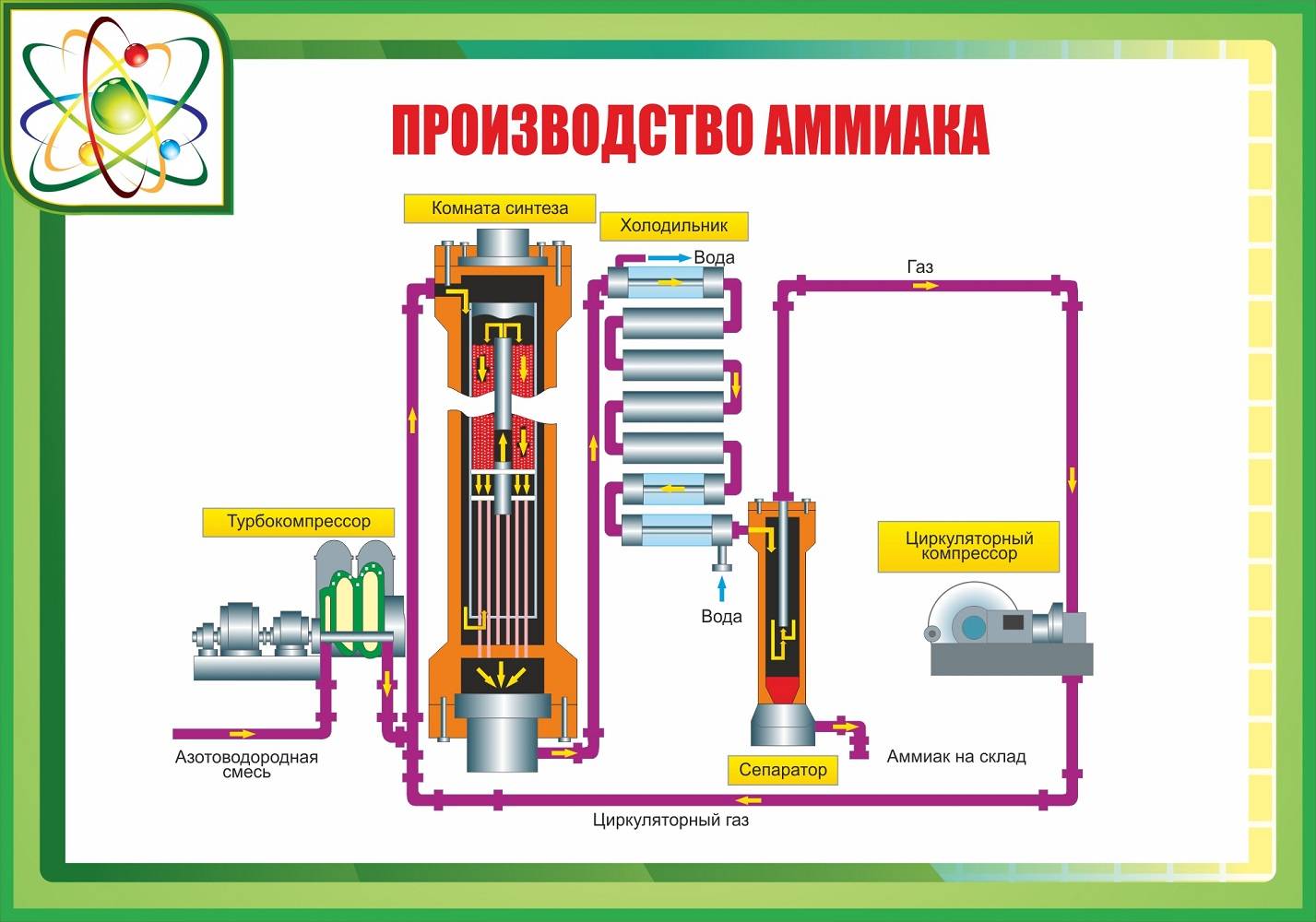
Производство аммиака
Современное производство
Система работы любого аммиачного завода достаточно сложная и содержит в себе нескольких этапов. Технология получения искомого вещества осуществляется в 6 этапов. В процессе проведения синтеза происходит получение, собирание и распознавание аммиака.
Первоначальная стадия заключается в извлечении серы из природного газа при помощи десульфуратора. Эта манипуляция требуется вследствие того, что сера является каталитическим ядом и убивает никелевый катализатор еще на стадии извлечения водорода.

На втором этапе проходит конверсия метана, которая протекает с применением высокой температуры и давления при использовании никелевого катализатора.
На третьей стадии случается частичное выгорание водорода в кислороде воздуха. В результате производится смесь водяного пара, оксида углерода, а также азота.
На четвертом этапе происходит реакция сдвига, которая проходит при различных катализаторах и двух отличных температурных режимах. Первоначально применяется Fe3O4, и процесс протекает при температуре 400 ˚С. Во второй стадии участвует более эффективный по своему воздействию медный катализатор, что позволяет осуществление производства при низких температурах.
Следующая пятая стадия предполагает избавление от ненужного оксида углерода (VI) из смеси газа путем применения технологии поглощения раствором щелочи.
На завершающем этапе оксид углерода (II) удаляется при использовании реакции конверсии водорода в метан через никелевый катализатор и большую температуру.
Полученная в результате всех манипуляций смесь газа содержит 75 % водорода и 25 % азота. Ее сжимают под большим давлением, а затем остужают.
Именно эти манипуляции описывает формула выделения аммиака:
Хоть этот процесс выглядит не очень сложным, однако все вышеперечисленные действия по ее осуществлению говорят о сложности получения аммиака в промышленном масштабе.
На качество конечного продукта влияет отсутствие в сырье примесей.
Пройдя долгий путь от небольшого лабораторного опыта до масштабного производства, получение аммиака на сегодняшний день является востребованной и незаменимой отраслью химической промышленности. Этот процесс постоянно совершенствуется, обеспечивая качество, экономичность и необходимое количество продукта для каждой ячейки народного хозяйства.
Аммиак: производство и использование
Возможно, вы припомните из школьного курса химии, что аммиак имеет очень простую формулу – NH3. Что касается физических свойств вещества – это бесцветный газ с резким запахом. Он хорошо растворим в воде: от 700 до 1200 объемов NH3 растворяется в одном объеме воды (в зависимости от температуры).
Синтез происходит путём соединения молекул азота с водородом в условиях высокой температуры и давления.
Этот процесс описывает следующая формула, которую впервые вывел немецкий физик Габер:
В формуле «кат.» – сокращение от слова «катализатор». В нашем случае речь идет о температуре, давлении и химических примесях. Q – это выход тепловой энергии, так как реакция экзотермическая.
Как мы ранее упоминали, синтез аммиака – это очень энергозатратный процесс. Он требует температуру порядка 400-500 градусов Цельсия и давление от 16 до 100 мегапаскаль.
Химические примеси, которые используют в качестве катализатора, — это восстановленное железорудное железо с К (Калием), Si (Силицием), Ca (Кальцием) или Al2O3 (оксидом алюминия). Ингибиторами при синтезе аммиака выступают вода, сернистый водород (H2S) и оксид углерода (CO/ CO2).
Помимо этого метода получения существуют еще два: дуговой и цианамидный.
| Метод получения аммиака | Описание | Затраты энергии на производство 1 т аммиака, кДж |
|---|---|---|
| Дуговой метод | Основывается на эндотермической реакции окисления азота кислородом, протекающей при температуре 3000 градусов Цельсия в пламени вольтовой дуги. | 7*104 |
| Дуговой метод | Основывается на способности измельченного карбида кальция реагировать с молекулярным азотом при температуре около 1000 градусов Цельсия. В результате образуется кальций цианамида, который после превращается в аммиак. | 1,2*104 |
По сравнению с дуговым и цианамидным методами, предложенный Габером вариант является самым энергетически выгодным. Затраты энергии для изготовления тонны продукта составляют всего 0,5*104. Именно поэтому данный способ – самый распространенный.
Ежегодно в мире изготовляется более 150 000 000 тонн аммиака. При этом значительная доля, как мы уже упоминали, идёт на сельскохозяйственные потребности – а именно на изготовление аммиачных удобрений.
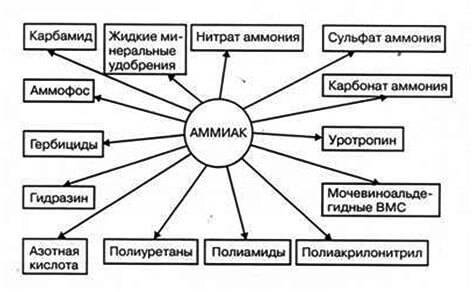
а) Главные производственные особенности
- Достичь 100% выхода продукта невозможно из-за высокого температурного порога протекания реакции. Максимально ожидаемый выход конечного продукта не превысит 40-45%. Минимальный выход аммиака составит всего 20%.
- Производственный процесс рециркулирует, то есть часть азота, которая не превратилась в продукт, охлаждается и повторно идёт на производство.
- Наличие катализатора не опционно, а обязательно.
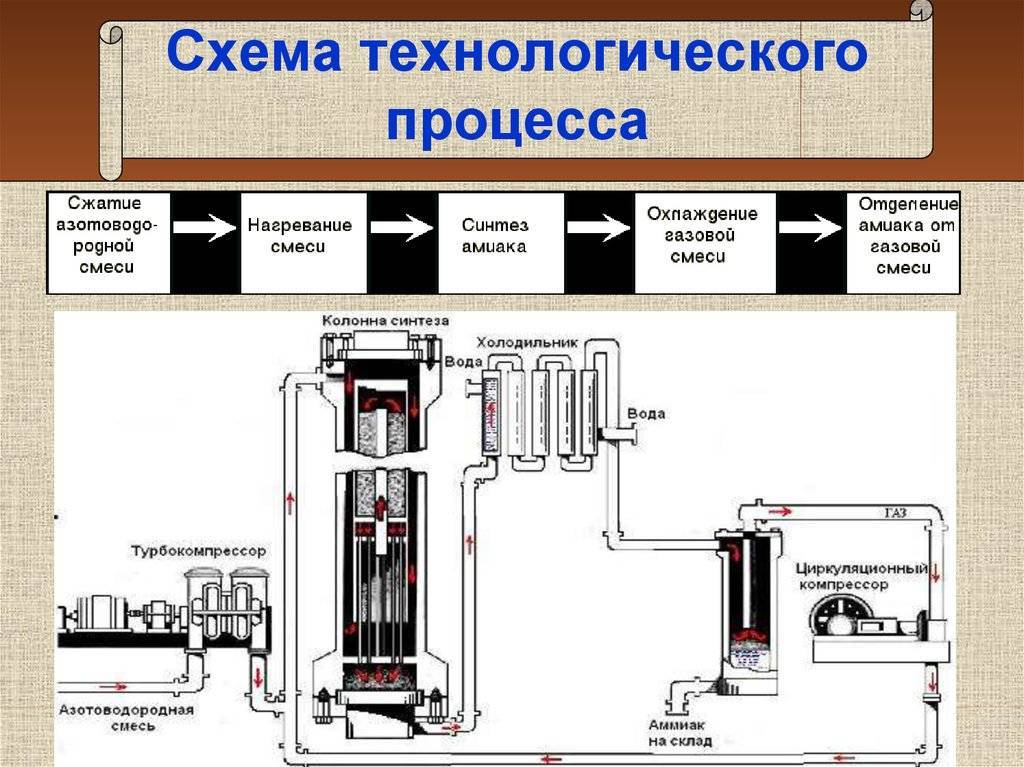
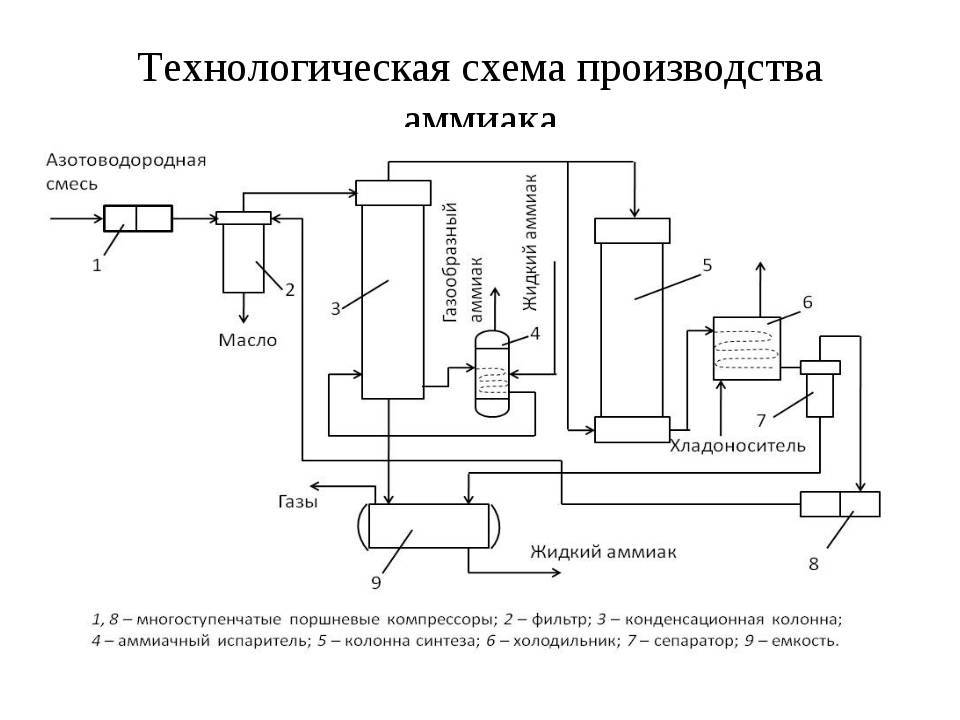
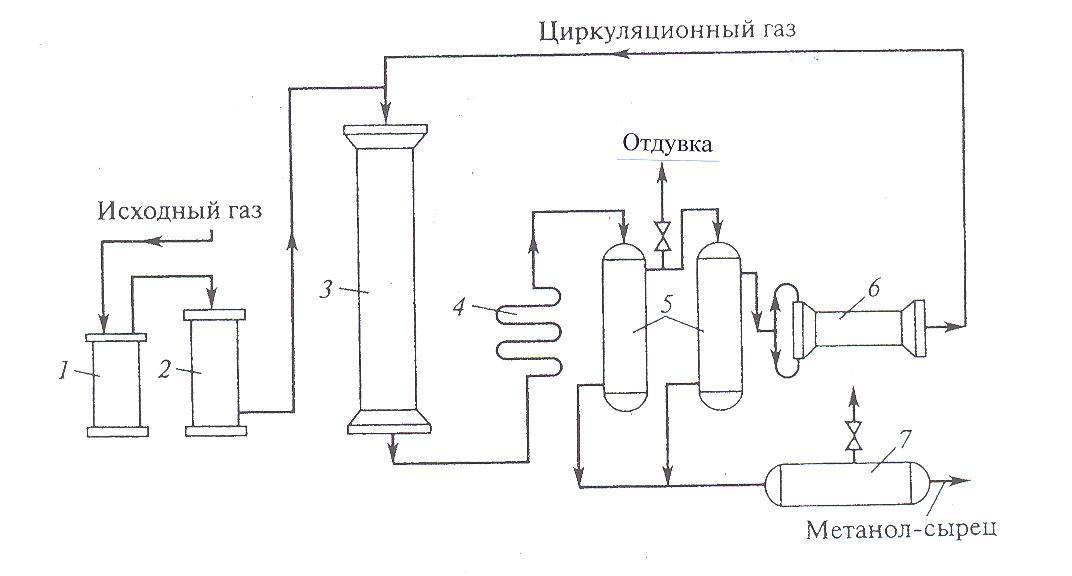
б) 6 этапов производства аммиака
| 1 этап | Подготовленную смесь азота и водорода подают по трубопроводу в компрессор. |
| 2 этап | После прохождения турбокомпрессора реакционная смесь подается в колонну синтеза, куда поступают химические катализаторы. |
| 3 этап | Весь полученный аммиак, который, в среднем, составляет 25% от теоретически возможного, подается в холодильный компартмент для охлаждения, так как в процессе синтеза смесь сильно нагревается вследствие экзотермической реакции. |
| 4 этап | Под воздействием давления аммиак из газообразного переходит в жидкое состояние. |
| 5 этап | В сепараторе происходит разделение конечного продукта реакции и непрореагировавшей смеси, которая рециркулирует в исходную точку производства через компрессор. Благодаря рециклизации используется до 96% всей азотноводородной смеси. |
| 6 этап | Жидкий аммиак поступает в отсек для хранения при контролируемых условиях. |
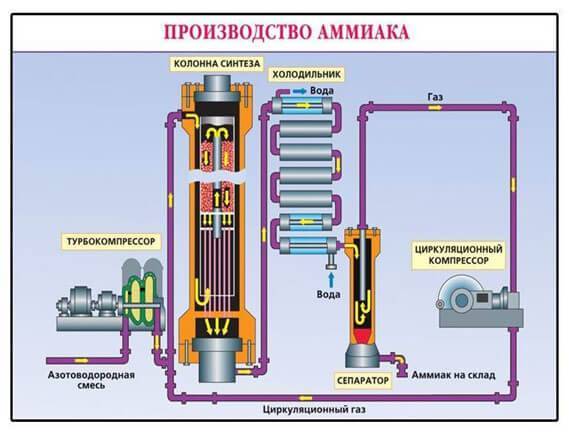
Производство аммиака почти безотходное благодаря системе повторного направления смеси в реактор. К тому же выход энергии от реакции частично покрывает необходимые температурные условия.
Чтобы вы могли лучше разобраться в процессе производства аммиака, предлагаем ознакомиться с коротким видео:
Производство аммиака
Азотное производство играет важнейшую роль в современной химической промышленности. Стоит заметить, что соединения азота применяются как при получении органических, так и неорганических веществ. Особую статью в азотной промышленности составляет производство аммиака. Именно при «участии» этого ценнейшего компонента производятся удобрения, азотная кислота, взрывчатые вещества, хладоагенты и многое другое. При всей своей полезности аммиак является довольно сильным ядом, несмотря на то что применяется в медицине в виде нашатыря.
Сам аммиак как вещество впервые был обнаружен в конце XVIII века. Описал его как отдельное вещество англичанин Джозеф Пристли. Спустя 11 лет французом Клодом Луи Бертолле был изучен химический состав этого вещества. Необходимость получения аммиака в промышленных количествах стала остро возникать в конце XIX века, когда стали истощаться месторождения чилийской селитры, из которой в основном получали азотные соединения. Именно «щелочной воздух» стал самым перспективным компонентом для производства различных химических соединений, которые оказали огромное влияние на разные стороны жизни человека: от военного дела, до сельского хозяйства.
Но эта проблема была решена только в начале XX столетия, когда появился способ производства аммиака путем прямого синтеза из азота и водорода. Таким образом, од возникновения проблемы до ее решения прошел довольно длительный период, в ходе которого было сделано несколько открытий, позволивших «сказку сделать былью».
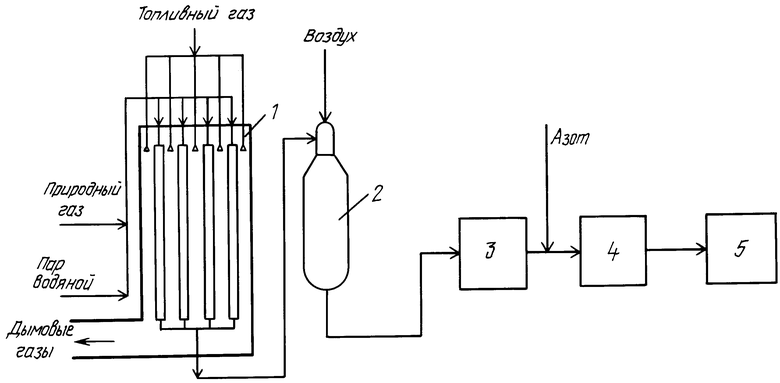
Производство газа технологического назначения

Данное производство является начальным этапом в синтезе аммиака и проводится под давлением около 30 ат. Для этого природный газ сжимается с использованием компрессора до 40 ат, далее он подогревается до 400 градусов в змеевике, который расположен в трубчатой печи, и подается в отсек сероочистки.
При наличии серы в количестве 1 мг в м в очищенном природном газе его нужно смешать с водяным паром в соответствующем соотношении (4:1).
Реакция взаимодействия водорода с окисью углерода (т.н. метанирование) происходит с выделением огромного количества тепла и значительным уменьшением объема.